Préparation microscopique de cellules de cristallin
Protocole permettant l'observation au microscope de coupes de cristallin
Matériel |
|
|
- Un œil
- Une cuvette à dissection
- Une paire de ciseaux fins ; une pince fine ; un scalpel
- Des gants
- Une lame et une lamelle ; un flacon bleu de méthylène ; un flacon d’eau distillée ; un microscope optique
- De l’essuie tout
|
|
|
|
|
- Couper le cristallin en deux à l’aide du scalpel.
- Prélever un fragment de cristallin à l’aide de la pince, le déposer dans une goutte d’eau sur une lame, ajouter une goutte de bleu de méthylène.
- Dilacérer le fragment à l’aide d’une pince fine.
- Déposer la lamelle.
- Observer au microscope.
|
|
En images
 |
 |
|
1-couper le cristallin en deux. |
2-Prélever un fragment |
 |
 |
|
3-Déposer le fragment dans l'eau |
4-Ajouter une goutte de bleu de méthylène |
 |
 |
| 5-Dilacérer |
6-Déposer une lamelle |
Le résultat au microscope
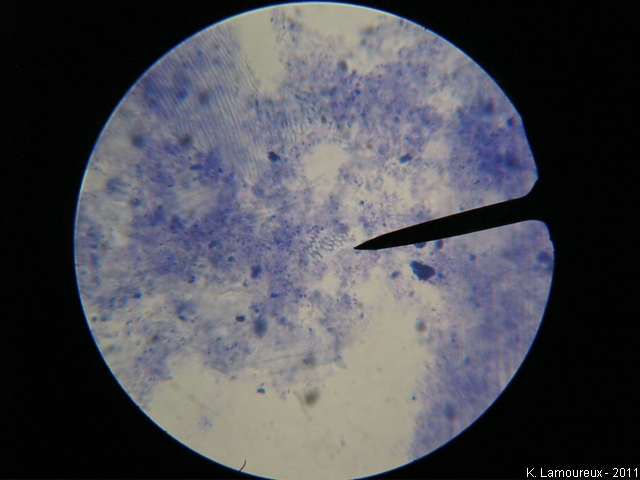
X4X16
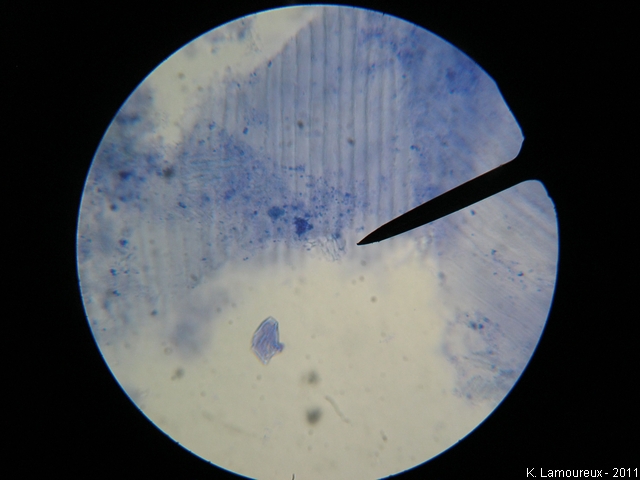
X10X16

X40X16
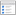
En balayant la lame, on observe très nettement les fibres constitutives du cristallin, aussi bien en coupe longitudinale (amas de fibres jointives parallèles) qu’en coupe transversale (amas d’hexagone).
Trucs et astuces
- La mise en évidence de l’effet loupe peut se faire en posant une lame à concavité sur le cristallin et en exerçant une pression plus ou moins forte.
- Pour la préparation microscopique, les deux clés de la réussite sont la coloration et la dilacération des fibres du cristallin.
- Pour la coloration, en présence de trop de bleu de méthylène, les cellules sont trop foncées, nous proposons donc de mettre le fragment dans l’eau et d’ajouter du bleu de méthylène pour obtenir une coloration suffisante mais non excessive. Cette remarque ne vaut que si le bleu de méthylène est concentré, il faudra donc veiller à tester la coloration.
- Pour la dilacération, nous avons essayé deux techniques : dilacérer dans le liquide à l’aide d’une pince fine directement sur la lame ou appuyer sur la lamelle (éponger les débordements) ; cette dernière technique permet d’obtenir de bons résultats mais les fibres sont bien plus courtes que lorsque l’on dilacère.
Réalisé par Isabelle Dégardin-Wiart (ATPL) et Karine Lamoureux (enseignante)
(lycée Paul Duez, Cambrai)